Recuperación de fluorita de los relaves de flotación
Por: D. Tamayo-Soriano (a), F. R. Carrillo-Pedroza (a), E. E. Guel-Cruz (b), M. J. Soria-Aguilar (b), A. Martínez Luevanos (a)
Resumen
Los jales, relaves o colas del proceso de concentración de fluorita, contienen concentraciones de elementos como el flúor (de la fluorita) en algunos lugares, presencia de berilio y tierras raras como neodimio, cerio, lantano y disprosio, entre otras. Debido a las grandes cantidades de residuos, depositados en las presas de jales y a la cada vez mayor demanda de nuevos materiales para la generación de energías limpias, y en el marco de la economía circular, estos residuos pueden ser una fuente atractiva de elementos valiosos, que además permite el aprovechamiento integral de los recursos naturales. En este sentido, es necesario generar el conocimiento fundamental que permita valorar y evaluar la posibilidad de extraer estos elementos de los mencionados residuos. El objetivo de este trabajo es llevar a cabo la optimización de un determinado número de pruebas de flotación, que permitan obtener valores interesantes de recuperación de fluorita. El mineral utilizado proviene de la región centro Norte del Estado de Coahuila. La ley de cabeza de los relaves estudiados fue de un 35.72 % en CaF2 y el hecho de ser un subproducto a gestionar, hacen interesante su flotación. El tamaño de partícula fue 0.106 mm, obtenida después un proceso de molienda. Las pruebas se acondicionaron durante un total de 7 minutos a 60 °C y 80 °C, ajustando el pH entre 9 y 10 con hidróxido de sodio. Se utilizaron quebracho, almidón y dextrosa como depresores de los carbonatos de calcio, silicato de sodio como depresor de la sílice y ácido oleico como colector de la fluorita. Los análisis elementales de las pruebas de flotación se llevaron a cabo por la técnica de fluorescencia de rayos X (FRX). Los resultados de flotación muestran que se obtuvieron concentrados de 50.72 % y 73.90 % como mejor resultado, con valores de recuperación desde 56.04 % y 88.63 %.
Palabras clave: Fluorita; relaves; flotación
Abstract
The tailings of the fluorite concentration process contain concentrations of elements such as fluorine (from fluorite) in some places, the presence of beryllium and rare earths such as neodymium, cerium, lanthanum and dysprosium, among others. Due to the large amounts of waste, deposited in tailings dams and the increasing demand for new materials for the generation of clean energy, and within the framework of the circular economy, this waste can be an attractive source of valuable elements, which also allows the integral use of natural resources. In this sense, it is necessary to generate the fundamental knowledge that allows assessing and evaluating the possibility of extracting these elements from those mentioned. The objective of this work is to carry out an optimization of a certain number of flotation tests, which obtain interesting values of fluorite recovery. The mineral used comes from the North central region of the State of Coahuila. The head grade of the studied tailings was 35.72% in CaF2 and the fact that it is a by-product to be managed makes its flotation interesting. The particle size was 0.106 mm, obtained after a milling process. The tests were conditioned for a total of 7 minutes at 60 ° C and 80 ° C, adjusting the pH between 9 and 10 with sodium hydroxide. Quebracho, starch and dextrose were used as calcium carbonate depressants, sodium silicate as silica depressant and oleic acid as fluorite collector. The elemental analyzes of the flotation tests were carried out by the X-ray fluorescence technique (XRF). The flotation results showed that concentrates of 50.72% and 73.90% were obtained as the best result, with recovery values from 56.04% and 88.63%.
Key words: Fluorite; Tailings; Flotation
Introducción
La fluorita (CaF2) es un mineral compuesto por 48.67% de flúor y 51.33% de calcio. De forma comercial también se le conoce como espato-flúor (fluorspar). Es un mineral de gran importancia a nivel mundial, y está incluido actualmente dentro de las veintisiete materias primas críticas (Critical Raw Material – CRM) (Hetherington y Bloodworth, 2008), dado que los riesgos de escasez de suministro y los efectos que ejercen sobre la economía son más importantes que los de la mayoría de las demás materias primas (European Commission, 2017). También es considerado como crítico por otros países como China y EEUU (Cai, 2016). A nivel mundial, los principales extractores son China y México (Tercero-Espinoza et al., 2015).
De acuerdo con el USGS, en 2019, la producción mundial de fluorita fue de 7 millones de toneladas, un aumento de 280 mil toneladas con respecto a 2018. A nivel mundial se pronostica mayor demanda tanto de fluorita grado metalúrgico como de concentrado de grado ácido. El mayor productor de fluorita en el mundo es China con el 57% de producción mundial, mientras que México ocupa el segundo lugar con 17.1% de participación. En nuestro país, durante 2019 de acuerdo con el INEGI, se produjeron 1.23 millones de toneladas de fluorita, con un aumento de 4.2% con respecto al año anterior, su valor tuvo una contracción de 11% colocándose en 3 mil 400 millones de pesos (Camimex, 2021).
La fluorita se comercializa en tres grandes grupos, en función de su contenido en CaF2:
- Grado ácido: Contenido superior al 97% de CaF2. Es la principal fuente industrial de flúor y ácido fluorhídrico (HF).
- Grado metalúrgico: Contenido superior al 70% de CaF2.
- Grado cementero: Contenido superior al 35% de CaF2.
Los yacimientos de fluorita coexisten con diferentes minerales considerados de menor valor (ganga), como el cuarzo (Chen et al., 2019), la calcita o la dolomita (Foucaud et al., 2019; Zhu et al., 2018) y la barita (Slaczka, 1987). El tipo de mineralización más común son los depósitos en rocas sedimentarias, principalmente en carbonatos (carbonate-hosted lead-zinc deposits), cuyo modelo de formación responde a las características de los yacimientos de tipo Mississippi Valley (MVT) (Sangster, 1996).
En el caso particular de los yacimientos de fluorita en Coahuila, uno de los más interesantes son los ubicados en la zona centro Norte del Estado. En esta zona se identifican formaciones geológicas de tipo calderas colapsadas que están rodeadas por cúpulas de riolita. Los diques anulares de riolita y basanita rodean la cúpula y los reemplazos se encuentran en las calizas adyacente a los diques de riolita que contienen fluorita, calcita, cuarzo, hematita, limonita y cantidades menores de aragonita, powellita, adularia, caolinita, yeso, sericita y bertrandita (mineral de berilio), así como la coexistencia de algunos depósitos de elementos del grupo Lantánidos, conocido como elementos de tierras raras o REE (siglas en ingles de rare earth elements) relacionados con minerales como la bastnasita, (McLemore, 2018).
Bajo este contexto, dada la asociación de minerales con la fluorita, el proceso de concentración de este mineral conlleva la generación de un concentrado de fluorita, generalmente grado ácido, y como subproducto o relaves del proceso, un material rico aun con buenos contenidos de fluorita. Aunque no es el objetivo de este trabajo, es importante mencionar que, dado que el proceso de concentración es muy selectivo en cuanto a producir fluorita de alta pureza, los relaves (colas o jales) aun contienen concentraciones importantes de este mineral, junto con los carbonatos con contenidos de REE, y cuarzo. Este trabajo se centra en estudiar el procesamiento que permita la recuperación de los valores de fluorita contenidos en los relaves del proceso de concentración de dicho mineral.
Metodología
El material de fluorita utilizado para este trabajo proviene del Norte del Estado de Coahuila, México. Es importante mencionar que el material utilizado para las pruebas de flotación es una muestra de relaves de flotacion de una planta de concentración de fluorita ya instaladas en el yacimiento.
El primer paso fue llevar a cabo la caracterización del mineral, Tabla 1. Se determinó la composición elemental mediante la técnica de Fluorescencia de Rayos X, con el objetivo de poder identificar los elementos de mayor abundancia del material de estudio. Para esto, se empleó un equipo de fluorescencia de Rayos X Panalytical modelo Epsilon, de la Universidad Autónoma de Coahuila. Con los datos se realizó la reconstrucción mineralógica, un previo procedimiento de lavado ácido, para discriminar e identificar el calcio correspondiente a la fluorita y a los carbonatos de calcio.

A continuación, puesto que el tamaño de partícula no es el adecuado para el proceso de flotación, se procedió a triturar, pulverizar y moler el material en un molino de bolas por un periodo máximo de 2 horas. Posteriormente, se tamizó el material en seco mediante mallas a diferentes fracciones de tamaños hasta alcanzar partículas de 0.106 mm, o que el material se encontrara por debajo de la malla 150, esto con el objetivo de liberar las especies minerales de interés. Este hecho influirá de forma positiva en la flotación, haciendo necesaria una menor dosificación de reactivos durante el proceso.
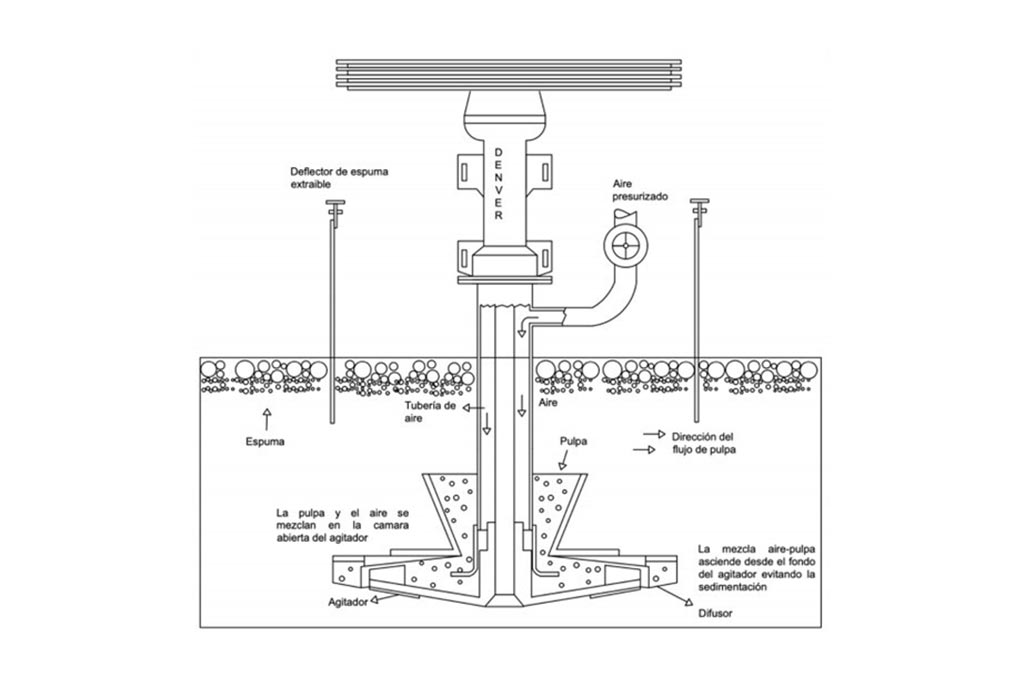
Las pruebas de flotación del mineral de fluorita se realizaron en una celda mecánica (tipo Denver), como se muestra en la Figura 1, usando una concentración de sólidos en la pulpa de mínimo un 25%. El sistema más empleado en la flotación de fluorita es el sistema ácido oleico (colector) – quebracho (depresor), acondicionado con silicato de sodio, a un pH entre 9 y 10, y a temperatura por arriba de los 40 °C.
Por otro lado, Zhao et al. (2013) determinaron que el punto de carga cero (PZC) para la fluorita es de 9.5 y para la calcita o carbonato cálcico 8.5 de esta forma, para evitar la flotación de carbonato cálcico los autores sugieren trabajar a pH por encima de 9, estando el óptimo comprendido entre 9.5-10. El valor utilizado de pH en el presente trabajo fue 9.5 ajustado con NaOH.
Se llevaron a cabo una serie de pruebas en una Celda de flotación, con las condiciones de dosificación de reactivos reportadas en la literatura, para la separación y recuperación de mineral de fluorita.
Kowalczuk et al. (2016) realiza la dosificación de reactivos por separado y estudia el tiempo de acondicionamiento para la formación de las fases presentes en el proceso de flotación.
En el presente trabajo, por el contrario, todos los reactivos fueron dosificados al mismo tiempo a excepción del ácido oleico. La velocidad del agitador se fijó en 1000 rpm. Para cada flotación, se utilizaron 300 g de mineral en 1 litro de agua. Después de ajustar el pH a 9.5 se añadieron los reactivos depresores y colectores. Las pruebas se acondicionaron durante un total de 7 minutos. El tiempo de dosificación fue de 5 minutos para los reactivos añadidos al mismo tiempo y dos minutos para el ácido oleico. El tiempo de flotación se fijó en 5 minutos o, hasta que se dejara de producir espuma dentro de la celda. La espuma, obtenida tras cada experimento, fue recogida por la parte superior de la celda con un rascador sobre una bandeja metálica. Dicha espuma se filtró y secó a 100ºC, se pesó y se analizó mediante la FRX.
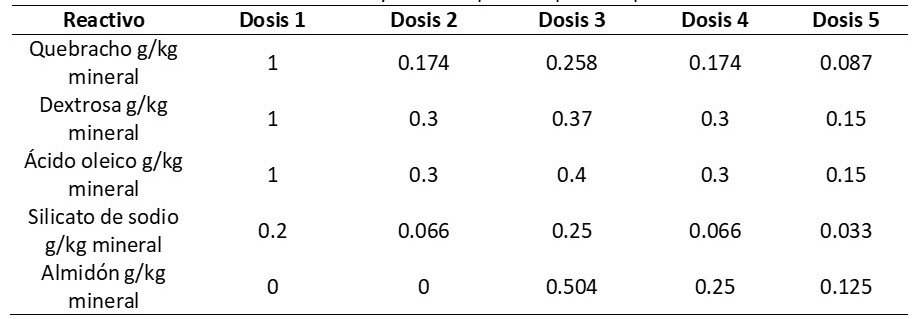
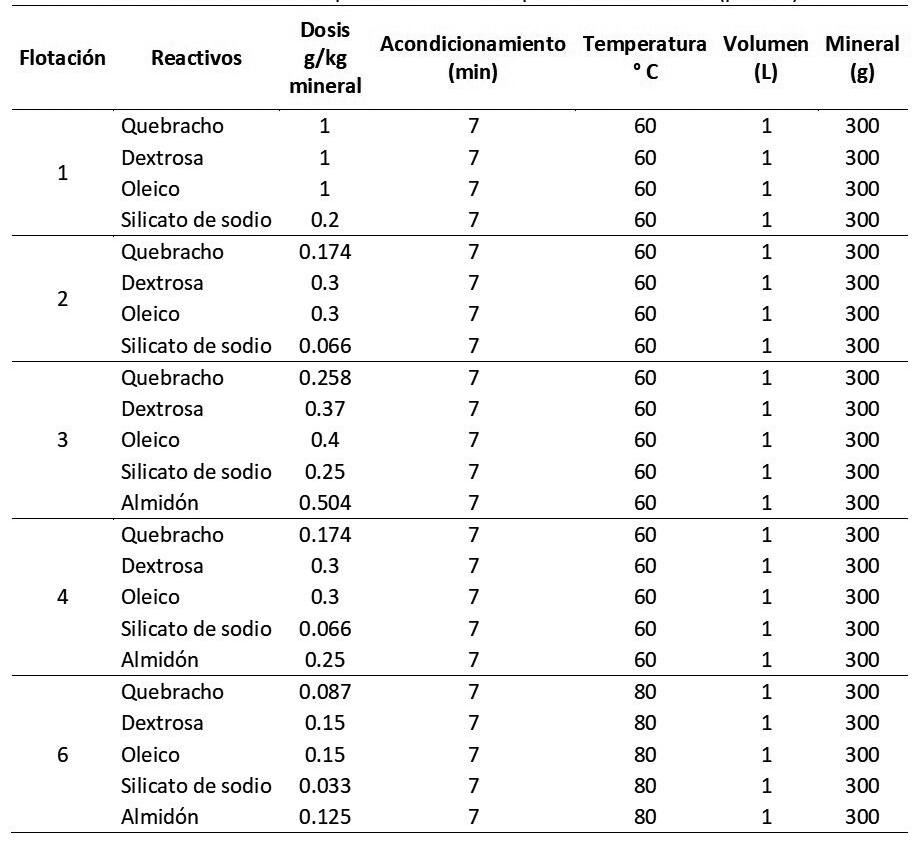
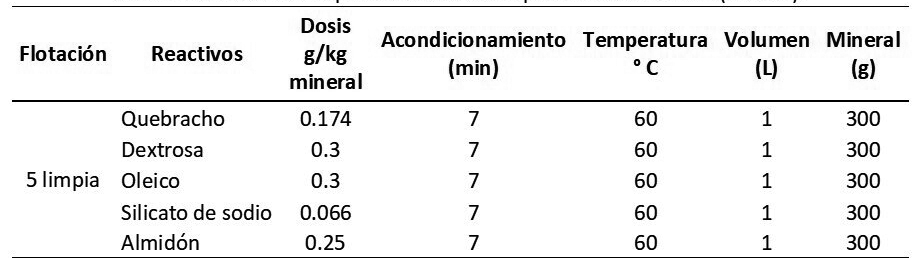
Las condiciones experimentales y reactivos utilizados para cada una de las flotaciones realizadas, se muestran en la Tabla 2, 3 y 4:
Resultados
La flotación1, permite obtener un concentrado con un 57.54 % de recuperación, empleando una temperatura de 60 °C. Los resultados también demuestran que es posible obtener una buena concentración de fluorita disminuyendo la dosificación de reactivos.
Para el caso de la Flotación 2, los reactivos empleados fueron exactamente los mismos que los utilizados para la Flotación 1, sin embargo, su dosificación fue menor. Permitió elevar a 73.90 % el concentrado de CaF2 y obtener una recuperación de 56.04 %.
Para la siguiente prueba (Flotación 3), se aumentó la dosificación de los principales reactivos empleados, pero ahora agregando almidón en un 0.504 g/kg. De esta prueba, los resultados muestran que la ley del concentrado de fluorita disminuyó a 54.09% pero la recuperación aumentó hasta un 77.98 %. Boulanger et. al. (2019), mencionan que la eficiencia de recuperación se maximiza cuando se aumenta tanto la temperatura como la adición de silicato de sodio, que para esta prueba se dosificó 0.25 g/kg.
Con respecto a la Flotación 4, se utilizaron los valores de dosificación de la Flotación 2 pero agregando de igual forma almidón a la mitad de lo utilizado para la Flotación 3, obteniendo hasta un 88.63 % de recuperación de fluorita. De estas dos últimas pruebas de flotación (Flotación 3 y 4), se utilizaron 150 g de cada una para realizar una limpia. Los 300 g utilizados (Flotación 5), se acondicionaron bajo la dosis con mejor respuesta obtenida en los valores de recuperación, dichos valores fueron tomados de la Flotación 4.
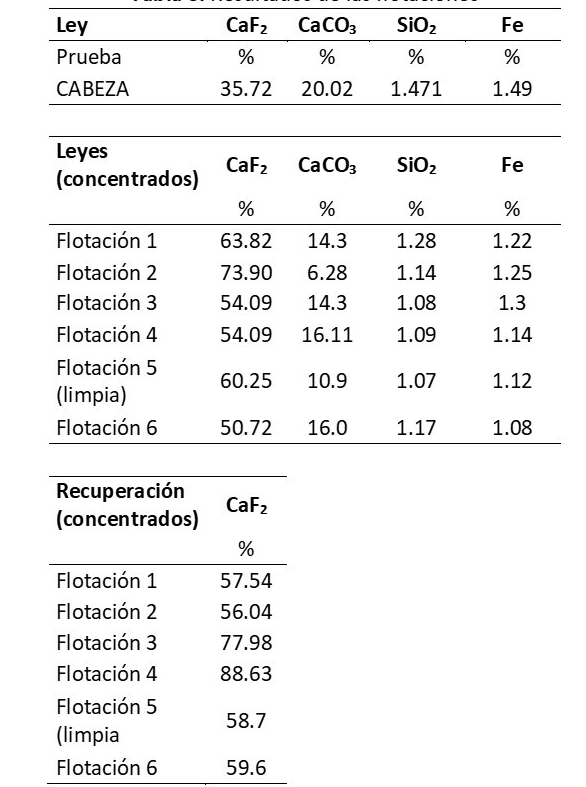
La Flotación 6, fue acondicionada a la mitad de reactivos de la limpia correspondiente a la Flotación 5 y aumentando la temperatura a 80 °C. Se observó que la temperatura de 80 °C en combinación con la cantidad de dosis utilizada, disminuye la ley de CaF2 considerablemente, sin embargo, se logró obtener la tercera mejor recuperación (59.6 %).
En resumen, el uso de altas temperaturas provocó una disminución significativa tanto en el contenido y recuperación de fluorita. En la Tabla 5, se muestran los resultados más significativos de las pruebas de flotación.
Conclusiones
- Para este trabajo, el uso de los reactivos comúnmente utilizados para la flotación de fluorita como son: Quebracho, Dextrosa, Ácido Oleico y Silicato de Sodio, promueven una recuperación de fluorita de hasta un 88.63 %, en una cabeza con ley del 35.72 %.
- La adición de almidón como acondicionador complementario a la dextrosa, tiene un efecto directo sobre el aumento de las leyes y su recuperación. De igual forma, el realizar una limpia a los concentrados (Flotación 5), no significó un cambio significativo en la ley del concentrado, ni en los porcentajes de recuperación.
- El aumento de la temperatura a 80 °C, demostró un gran decremento en la ley del concentrado de la Flotación 6.
Agradecimientos
El autor agradece a la Facultad de Metalurgia de la Universidad Autónoma de Coahuila por proveer todos los materiales necesarios y equipos de análisis.
Referencias
- Boulanger, J. F., Bazin, C., & Turgeon, K. 2019. Effect of Depressants and Temperature on Bastnaesite and Monazite Flotation Separation from a Canadian Rare Earth Element (REE) Ore. Minerals, 9(4), 225.
- Cai, H. 2016. Evaluation of fluorite resources and suggestions for industrial development, in: Proceedings of the 4th Academic Conference of Geology Resource Management and Sustainable Development. pp. 575–579
- Chen, W., Chen, Y., Bu, X., Long, T., Zhang, G., Chen, F., & Song, Y. 2019. Rheological investigations on the hetero-coagulation between the fine fluorite and quartz under fluorite flotation-related conditions. Powder Technology, 354, 423-431.
- European Commission (EC). 2017. Study on the review of the list of Critical Raw Materials. Luxembourg.
- Foucaud, Y., Filippova, I. V., & Filippov, L. O. 2019. Investigation of the depressants involved in the selective flotation of scheelite from apatite, fluorite, and calcium silicates: Focus on the sodium silicate/sodium carbonate system. Powder technology, 352, 501-512.
- Hetherington, L., & Bloodworth, A. 2008. Industrial minerals production in Europe: current situation and future trends. Industrial Minerals, (497), 56-61.
- Informe Anual :: Camimex. 2021. Retrieved 6 May 2021, from https://www.camimex.org.mx/index.php/publicaciones/informe-anual/informe/90
- McLemore, V. T. 2018. Rare earth elements (REE) deposits associated with great plain margin deposits (alkaline-related), southwestern united states and eastern mexico. Resources, 7(1), 8.
- Mackay, I., Videla, A. R., & Brito-Parada, P. R. 2020. The link between particle size and froth stability-Implications for reprocessing of flotation tailings. Journal of Cleaner Production, 242, 118436.
- Rutledge, J., & Anderson, C. G. 2015. Tannins in Mineral Processing and Extractive Metallurgy. Metals, 5(3), 1520-1542.
- Ślaczka, A. S. 1987. Effects of an ultrasonic field on the flotation selectivity of barite from a barite-fluorite-quartz ore. International Journal of Mineral Processing, 20(3-4), 193-210.
- Tercero Espinoza, L., Hummen, T., Brunot, A., Hovestad, A., Peña Garay, I., Velte, D., … & Joce, C. 2015. Critical raw materials substitution profiles. CRM InnoNet: Karlsruhe, Germany.
- Wills, B. A., & Finch, J. 2006. Wills’ mineral processing technology: an introduction to the practical aspects of ore treatment and mineral recovery. Publisher: Butterworth-Heinemann, 12, 266-344.
- Zhang, G., Gao, Y., Chen, W., & Liu, D. 2017. The Role of Water Glass in the Flotation Separation of Fine Fluorite from Fine Quartz. Minerals, 7(9), 157.
- Zhu, H., Qin, W., Chen, C., Chai, L., Jiao, F., & Jia, W. (2018). Flotation separation of fluorite from calcite using polyaspartate as depressant. Minerals Engineering, 120, 80-86.
(a) Facultad de Ciencias Químicas, Universidad Autónoma de Coahuila, Saltillo, México
(b) Facultad de Metalurgia, Universidad Autónoma de Coahuila, Monclova, México


















